Vous êtes-vous déjà demandé comment les entreprises pharmaceutiques s'assurent que chaque médicament est sûr et fiable ? La conformité ne se résume pas à des formalités administratives. C'est un élément essentiel pour protéger les patients et préserver la confiance.
Cela implique l'adoption des BPF dans l'industrie pharmaceutique pour réglementer les entreprises du secteur de la santé. Ces bonnes pratiques « x » Les normes de pratique guident la manière dont les médicaments sont développés, fabriqués et testés.
Cela étant dit, explorons ce que c’est et pourquoi c’est important pour l’industrie pharmaceutique.
Qu'est-ce que GxP dans l'industrie pharmaceutique ?

Dans l'industrie pharmaceutique, les BPF désignent un ensemble de directives et de réglementations de qualité qui garantissent la sécurité, l'efficacité et la fiabilité des médicaments. « GxP » signifie Bonnes pratiques « x », où « x » peut désigner différents domaines tels que fabrication pharmaceutique, en laboratoire ou lors d'essais cliniques.
Ces normes sont reconnues dans le monde entier et sont appliquées par des organismes de réglementation comme le FDA aux États-Unis et le L'EMA en Europe.
L'objectif des BPF est de garantir que chaque étape du développement pharmaceutique respecte des règles strictes. En suivant ces directives, les entreprises peuvent protéger les patients, réduire les risques de contamination et instaurer la confiance avec les autorités réglementaires.
Importance des BPF dans l'industrie pharmaceutique
Les BPF sont un cadre qui affecte les patients, les entreprises et les régulateurs. Voici pourquoi elles sont importantes pour les entreprises :
1. Assure la sécurité des patients et la qualité des produits
La sécurité est au cœur de GxP, car les entreprises souhaitent des médicaments réellement efficaces et sans danger pour la santé. GxP s'assure que chaque comprimé, injection ou vaccin est fabriqué avec soin. Elle vérifie également les ingrédients, les étapes de production et les conditions de stockage.
Si ces étapes sont ignorées, des erreurs peuvent se produire et les patients peuvent tomber malades ou recevoir des médicaments inefficaces.
2. Protège les entreprises contre les risques juridiques et les rappels
La conformité aux BPF protège également les organisations contre d'importants risques juridiques et financiers. Le non-respect de ces normes peut entraîner des amendes réglementaires, des rappels de produits et une atteinte à leur réputation.
Par exemple, en 2012, Johnson & Johnson Plus de 135 millions de bouteilles ont été rappelées et des problèmes de contrôle qualité ont été constatés. Cela démontre l'importance du respect des normes GxP pour minimiser ces risques et les rappels de produits.
3. Établit la confiance avec les régulateurs et les patients
Le respect des BPF témoigne d'un engagement envers la qualité et l'intégrité réglementaire. Les organismes de réglementation, notamment la FDA et l'EMA, s'appuient sur ces normes pour évaluer les pratiques opérationnelles.
La conformité signale aux autorités réglementaires et aux patients que les processus sont fiables et contrôlés. Cette confiance est cruciale, car elle sous-tend l'autorisation de mise sur le marché, la confiance des parties prenantes et la crédibilité à long terme de la marque.
Quels sont les éléments fondamentaux des BPF dans l’industrie pharmaceutique ?
Les BPF ne sont pas une norme unique. Il s'agit d'un ensemble de pratiques complémentaires couvrant différents domaines du développement et des opérations pharmaceutiques. Chaque élément a un objectif spécifique, mais fonctionne de concert pour garantir la qualité, la sécurité et la conformité.
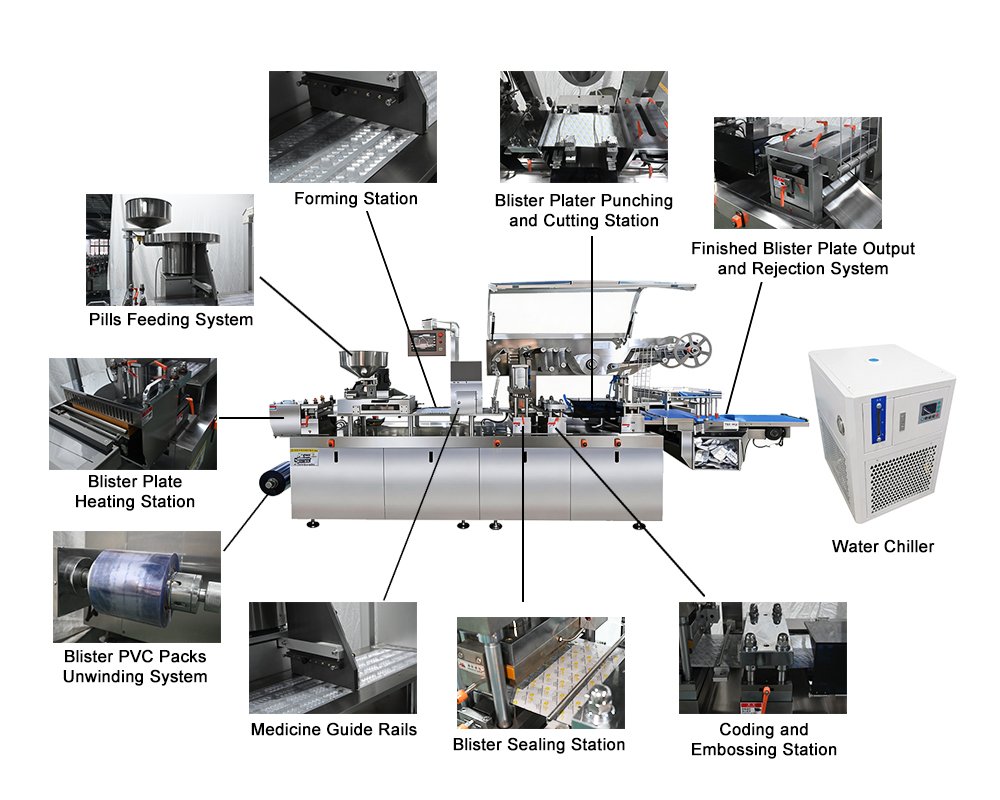
1. Bonnes pratiques de fabrication (BPF)
Les BPF visent à contrôler les produits pharmaceutiques et à garantir qu'ils sont produits et contrôlés de manière constante, conformément aux normes de qualité. Elles couvrent toutes les étapes, de l'approvisionnement en matières premières à l'emballage et à l'étiquetage.

Cela comprend l'étalonnage des équipements, la formation du personnel, la documentation et les normes d'hygiène. BPF contribue à prévenir la contamination, les erreurs et la variabilité entre les lots. En bref, c'est la base d'une fabrication fiable.
2. Bonnes pratiques de laboratoire (BPL)
Les BPL régissent la planification, la conduite, le suivi et la communication des études en laboratoire. Elles garantissent la reproductibilité et l'exactitude des expériences, des tests et des analyses.

Par exemple, les études de stabilité ou les tests chimiques doivent respecter les règles des BPL pour produire des données fiables. Si vous êtes un chercheur, vous devez respecter ces normes.
3. Bonnes pratiques de laboratoire clinique (BPC)
Le GCLP se concentre sur les essais cliniques et garantit que les études impliquant des sujets humains sont éthiques, sûres et scientifiquement fondées. Il établit des normes pour la conception des études, le consentement éclairé, l'intégrité des données et le suivi.

La conformité aux GCLP protège les participants tout en générant des données fiables issues des examens réglementaires. Il est crucial de respecter les normes GCLP, car elles garantissent que les nouveaux médicaments sont testés correctement avant leur mise sur le marché.
4. Bonnes pratiques de documentation (GDocP)
Le GDocP vérifie que tous les dossiers, rapports et données sont exacts, complets et traçables. De plus, il stipule que chaque action, observation et décision doit être clairement documentée par les entreprises.

Une documentation adéquate facilite les audits, les inspections et les soumissions réglementaires. Dans le secteur pharmaceutique, les GDocP préviennent les problèmes d'intégrité des données et renforcent la conformité globale aux BPF.
Avantages du respect des BPF dans l'industrie pharmaceutique
Voici ce qui se passe lorsque les entreprises se conforment aux pratiques GxP :
1. Réduction des rappels et des risques de conformité
Le respect des BPF réduit considérablement le risque de rappel de produits. Chaque étape, de la production aux tests, est surveillée et documentée. Ainsi, les entreprises peuvent détecter les problèmes avant que les produits n'atteignent les patients.
Les inspections réglementaires deviennent également plus fluides, car les processus et les enregistrements sont conformes et transparents.
2. Amélioration de la cohérence et de la sécurité des produits
Les BPF garantissent que chaque lot de médicaments répond aux mêmes normes élevées. Des processus et des contrôles qualité standardisés préviennent toute variabilité. Cette cohérence est essentielle à la sécurité des patients et à l'efficacité thérapeutique.
Qu'il s'agisse de comprimés, d'injections ou de vaccins, les pratiques GxP garantissent que chaque produit fonctionne comme prévu.
3. Amélioration de la réputation auprès des régulateurs
Le respect des BPF montre qu’une entreprise s’engage à fournir des produits de haute qualité. Régulateurs, comme la FDA ou l’EMA, considèrent les entreprises conformes comme fiables et responsables.
Les clients et les professionnels de santé gagnent également en confiance envers la marque, sachant que les produits sont toujours sûrs et efficaces. N'oubliez pas qu'une réputation bâtie sur le respect des BPF peut accélérer les approbations.
4. Économies à long terme
Bien que la mise en œuvre des BPF nécessite un investissement initial, elle permet de réduire les coûts à long terme. La mise en œuvre des BPF peut contribuer à réduire les coûts en prévenant les rappels, en évitant les amendes réglementaires et en minimisant les risques. production pharmaceutique erreurs.
À long terme, GxP crée un modèle commercial plus durable et prévisible, faisant de la conformité une décision intelligente.
Défis courants en matière de conformité aux BPF
Si les avantages sont évidents, plusieurs obstacles peuvent compliquer la mise en conformité. Connaître ces défis permet aux organisations de s'y préparer et d'y faire face efficacement. Découvrons les défis auxquels vous pourriez être confronté lors de la mise en conformité.
1. Exigences réglementaires complexes
Les normes GxP sont complexes et varient selon les régions et les organismes de réglementation. Par exemple, les organisations opérant à l'échelle mondiale doivent gérer les complexités liées à l'alignement simultané avec plusieurs cadres réglementaires.
Cette complexité décourage les entreprises et engendre de la confusion. Cependant, la non-conformité peut s'avérer extrêmement coûteuse. Institut Ponemon Il a également été signalé que les organisations qui ne parviennent pas à effectuer des audits de conformité internes sont confrontées à un coût moyen de non-conformité par habitant de $1,275.
2. Problèmes d'intégrité des données
Bien que la fiabilité des données soit primordiale pour la conformité aux BPF, des problèmes d'intégrité des données persistent. Ces préoccupations sont également soulignées dans plusieurs lettres d'avertissement émises par la FDA.
Par exemple, en 2021, des problèmes d’intégrité des données ont été cités dans 65% des lettres d'avertissement de la FDACela met en évidence la prévalence des problèmes persistants d’intégrité des données et souligne l’importance pour les entreprises comme la vôtre de conserver des entrées précises.

Renforcez vos opérations pharmaceutiques avec GxP
Aujourd'hui, il est essentiel de suivre les BPF dans l'industrie pharmaceutique. Cela réduit les risques, améliore la cohérence et renforce la confiance des autorités réglementaires et des clients. Le processus peut paraître complexe, mais avec un accompagnement adapté, il devient gérable et gratifiant.
Et c’est ce que nous faisons chez Finetech.
Nous offrons une gamme complète lignes de production et des machines personnalisées pour soutenir vos objectifs de conformité et opérationnels.
Contactez Finetech maintenant pour explorer des solutions qui renforceront votre conformité !
FAQ
1. Comment les petites entreprises pharmaceutiques peuvent-elles mettre en œuvre les GxP ?
Les petites entreprises pharmaceutiques sont confrontées à des ressources limitées. Par conséquent, si vous souhaitez mettre en œuvre les BPF, commencez par les secteurs à haut risque, comme la fabrication et les essais cliniques. Une fois ces secteurs conformes, vous pourrez déployer les mêmes pratiques dans le reste de l'organisation.
2. Que doit faire une entreprise en cas de violation des BPF ?
En cas de violation des BPF, agissez immédiatement. Recherchez la cause profonde, documentez les résultats et mettez en œuvre des mesures correctives et préventives. Informez les autorités réglementaires si nécessaire et revoyez les processus pour éviter toute récidive. Une action rapide et transparente peut réduire les sanctions et protéger la sécurité des patients.
Références :
BPF vs BPFc : ce que les fabricants doivent savoir aujourd’hui
Bonnes pratiques de fabrication (BPF) pour la fabrication pharmaceutique : votre guide complet.
Qu'est-ce que le GMP ? Comprendre les Produits Généraux de la Machine.
Qu'est-ce que GMP, GDP, FDA, DMF et CEP : comprendre les principales différences.
GxP dans l'industrie pharmaceutique : un guide complet de conformité.
Avis de droit d'auteur :
Vous ne pouvez pas reproduire, modifier, publier, afficher, transmettre ou exploiter de quelque manière que ce soit le contenu de ce site web, ni utiliser ce contenu pour constituer une base de données de quelque nature que ce soit, sans l'autorisation écrite expresse et préalable de Finetech Group. Pour obtenir l'autorisation d'utiliser le contenu, veuillez contacter : info@pharmamachinecn.com
Clause de non-responsabilité:
Les informations contenues dans cet article sont fournies à titre d'information générale uniquement. L'entreprise ne garantit pas l'exactitude, la pertinence, l'actualité ou l'exhaustivité des informations, et l'entreprise n'assume aucune responsabilité en cas d'erreur ou d'omission dans le contenu de cet article.