Bei der pharmazeutischen Terminologie handelt es sich um eine Sammlung komplexer, branchenspezifischer Jargons und Fachbegriffe. Diese Begriffe umreißen die Standards, Prozesse und Vorschriften, die die Konsistenz in der globalen medizinischen Entwicklung gewährleisten.

Die Kenntnis der richtigen pharmazeutischen Terminologie verleiht Ihrer Stimme Glaubwürdigkeit. Sie hilft Ihnen bei der Kommunikation mit Ärzten, Apothekern, Wissenschaftlern, Händlern und Lieferanten. All dies ebnet den Weg für fundierte Entscheidungen und eine produktive Zusammenarbeit in der gesamten Branche.
Um Ihnen dabei zu helfen, werden wir die wichtigsten Begriffe der Pharmaindustrie aufschlüsseln, die jeder Fachmann kennen sollte.
A
- Pharmazeutischer Wirkstoff: Eine API ist das Herzstück eines jeden Medikaments und sorgt für dessen therapeutische Wirkung. Er wird mit anderen Komponenten kombiniert, um eine Krankheit zu diagnostizieren, zu behandeln, zu heilen oder zu verhindern.
- Ampulle: Kleine, versiegelte Glasbehälter, die für sterile injizierbare Arzneimittel verwendet werden. Sie schützen empfindliche Flüssigkeiten vor Luft und Verunreinigungen.
- Tatsächliche Anschaffungskosten: AAC ist der Endpreis, den eine Apotheke für den Kauf eines Medikaments nach Abschlägen, Rabatten, Rückbuchungen und anderen Anpassungen zahlt.
- ANDA (Abbreviated New Drug Application): Ein ANDA wird bei der FDA eingereicht, um die Zulassung für eine generische Version eines bereits zugelassenen Arzneimittels zu erhalten, indem dessen Bioäquivalenz nachgewiesen wird.
B
- Blisterverpackung: Die Blister-Verpackung Maschinen versiegeln jede Tablette oder Kapsel in ihrem eigenen Hohlraum mit Plastik und Aluminiumfolie.
- Bioverfügbarkeit: Die Bioverfügbarkeit misst die Menge eines Arzneimittels, die den Blutkreislauf erreicht. Sie hängt von den physikalischen und chemischen Eigenschaften des Medikaments, der Art der Verabreichung, der Absorption, dem Stoffwechsel und der Ausscheidung ab.
- Bioäquivalenz: Sie vergleicht die Formulierung und die Bioverfügbarkeit von zwei Arzneimitteln, um festzustellen, ob sie denselben therapeutischen Nutzen haben.
C
- Klinische Studie: In klinischen Studien wird die Sicherheit und Wirksamkeit eines neuen Medikaments für die Zulassung durch die FDA getestet.
- Gefälschte Medizin: Es handelt sich um gefälschte oder illegal hergestellte Arzneimittel, die der Gesundheit der Verbraucher schaden können.
- Kapsel: A Kapsel ist eine Darreichungsform, die den Wirkstoff in einer Hülle aus Gelatine oder auf Pflanzenbasis enthält. Die Hülle löst sich im Magen-Darm-Trakt auf, und der Wirkstoff wird in den Blutkreislauf abgegeben.
- CCP (Kritische Kontrollpunkte): CCPs heben wichtige Schritte im Herstellungsprozess hervor, bei denen die Kontrolle entscheidend ist, um Kontaminationen und damit verbundene Gesundheits- und Sicherheitsprobleme zu vermeiden.
D
- Händler: Vertriebshändler lagern, verwalten und liefern Arzneimittel und fungieren als Brücke zwischen Herstellern und Verkäufern.
- DMF (Drug Master File): Ein DMF ist ein vertraulicher Antrag an die FDA. Es enthält Informationen zu Herstellungsverfahren, Rohstoffen, Einrichtungen, Verpackungsmaterialien und anderen relevanten Daten.
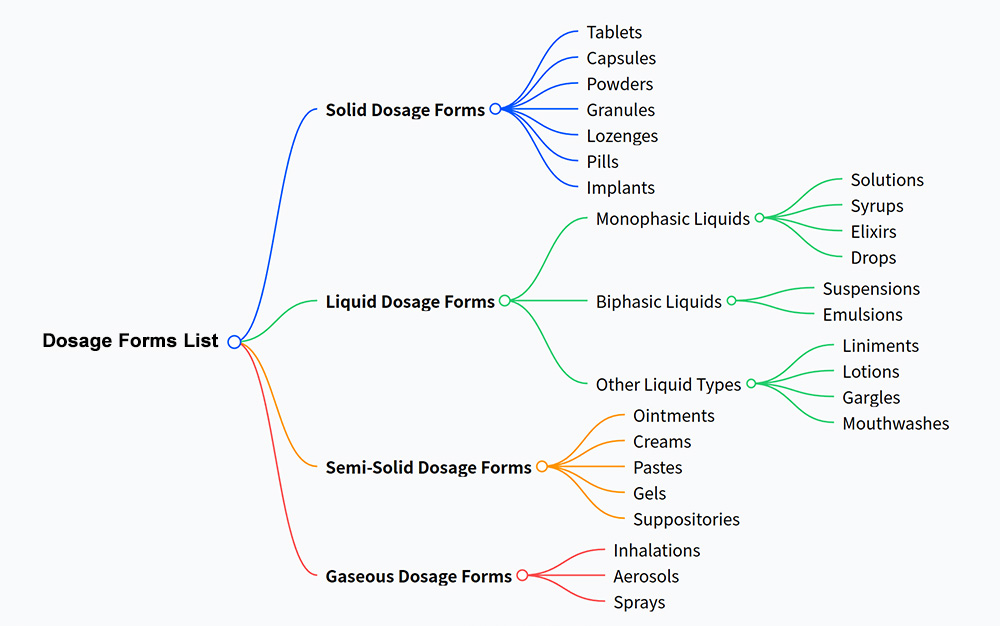
- Darreichungsform: Es handelt sich um die physische Form, in der ein Arzneimittel hergestellt und verabreicht wird, wie Tabletten, Kapseln, Salben oder Sirup.
- Droge Produkt: Ein Arzneimittel ist eine fertige Darreichungsform, die einen aktiven pharmazeutischen Wirkstoff (API) und inaktive Bestandteile (Hilfsstoffe) enthält.
E
- Hilfsstoff: Hilfsstoffe sind die inaktiven Komponenten, die die Eigenschaften des Wirkstoffs stabilisieren und verbessern.
- Verfallsdatum: Das Enddatum, bis zu dem das Arzneimittel unter den empfohlenen Lagerungsbedingungen wirksam und sicher bleibt.
- Endotoxin: Endotoxine sind toxische Substanzen, die von den äußere Membran von gramnegativen Bakterien.
F
- FDA: Die FDA ist die US-amerikanische Aufsichtsbehörde, die für die Sicherheit und Wirksamkeit von Arzneimitteln, Medizinprodukten, biologischen Produkten und Lebensmitteln zuständig ist.
- Formulierung: Dabei werden aktive und inaktive Bestandteile kombiniert, um ein stabiles und therapeutisch sicheres Endprodukt zu erhalten.
- Fertiges Produkt: Die endgültige Form eines pharmazeutischen Produkts, die alle Herstellungs-, Qualitätsprüfungs- und Verpackungsschritte durchlaufen hat.
G
- Generisches Medikament: Generische Arzneimittel denselben pharmazeutischen Wirkstoff (API) und dieselbe Bioäquivalenz wie das Markenarzneimittel enthalten.
- GMP (Gute Herstellungspraxis): Der GMP Verordnungen bieten einen Rahmen für die Formulierung, Verarbeitung und Verpackung von Arzneimitteln. Die Vorschriften stellen sicher, dass alle neuen und aktuellen Arzneimittel die Sicherheitsstandards zum Schutz der Patientengesundheit erfüllen.
- Gute klinische Praxis (GCP): GCP ist ein internationaler ethischer und wissenschaftlicher Qualitätsstandard für klinische Versuche mit Menschen.
H
- Homogenität: Die gleichmäßige Verteilung aller Bestandteile innerhalb einer Formulierung wird als Homogenität bezeichnet.
- Halbwertszeit: Die Halbwertszeit ist die Zeit, die vergeht, bis die Konzentration eines Arzneimittels im Körper auf die Hälfte des ursprünglichen Wertes gesunken ist.
I
- Identifizierung von Arzneimitteln (IDMP):Sie besteht aus fünf von der ISO aufgestellte Normen um eine einheitliche Kennzeichnung von Arzneimitteln in der ganzen Welt zu gewährleisten.
- IND-Antrag (Investigational New Drug): Es handelt sich um einen Antrag an die FDA, um die Genehmigung für klinische Versuche eines Prüfpräparats am Menschen zu erhalten.
- Zwischenbericht: Zwischenprodukte sind chemische Verbindungen, die bei der Herstellung eines Wirkstoffs entstehen. Sie durchlaufen weitere chemische Reaktionen, um zum fertigen pharmazeutischen Wirkstoff (API) zu werden.
J
- Just-in-Time-Fertigung: Dies ist eine Produktionsstrategie, die Verschwendung und Lagerkosten minimiert, indem pharmazeutische Produkte nur bei Bedarf hergestellt werden.
K
- Ketamin: Es handelt sich um ein Anästhetikum, das bei dissoziativer Anästhesie, Schmerzbehandlung und Depression eingesetzt wird.
L
- Bericht über die Losverteilung: Ein Bericht, der bei der FDA eingereicht wird, um die Menge der vertriebenen pharmazeutischen Produkte im Rahmen des Zulassungsantrags für biologische Arzneimittel (BLA) zu melden.
- Lyophilisierung: Die Gefriertrocknung ist ein Verfahren, bei dem pharmazeutischen Produkten Feuchtigkeit entzogen wird, vor allem durch Gefrieren und Sublimation, um ihre Stabilität und Haltbarkeit zu verbessern.
M
- Medizinprodukte: Medizinprodukte sind Instrumente, Apparate, Implantate und andere damit verbundene Ausrüstungen, die für medizinische Zwecke verwendet werden.
- Gegenseitiges Anerkennungsverfahren (MRP): Das Verfahren der gegenseitigen Anerkennung (Mutual Recognition Procedure, MRP) ist ein europäisches Zulassungsverfahren, das es ermöglicht, ein in einem EU-Mitgliedsstaat zugelassenes pharmazeutisches Produkt auch in anderen Staaten zuzulassen.
N
- Neue molekulare Entität: Ein neues Medikament, das einen Wirkstoff enthält, der noch nicht von der FDA zugelassen wurde.
O
- Freiverkäufliche Medikamente (OTC): Medikamente, die ohne Rezept in der Apotheke erhältlich sind, werden als rezeptfreie Arzneimittel bezeichnet.
- Orange Book: Die Orange Bookist eine Veröffentlichung der FDA, in der zugelassene Arzneimittel und ihre therapeutische Äquivalenz aufgeführt sind.
P
- Primärverpackung: Die Primärverpackung (Ampullen, Fläschchen, Blister), auch Verkaufsverpackung genannt, ist das erste Material, das direkt mit dem Arzneimittel in Berührung kommt.
- Patent: Ein Patent gewährt einem Unternehmen das ausschließliche Recht, ein neues Medikament herzustellen und zu verkaufen, in der Regel für 20 Jahre.
Q
- Qualitätskontrolle (QC): Dabei handelt es sich um ein System von Tests, Inspektionen und der Einhaltung von Vorschriften zur Erkennung und Vermeidung von Fehlern in der pharmazeutischen Produktion.
- Qualitätssicherung (QA)): Die Qualitätssicherung ist ein systematischer Prozess, der jede Phase der pharmazeutischen Produktion überwacht, um sicherzustellen, dass die Produkte den Qualitätsstandards entsprechen.
R
- Rx: Dieses Symbol leitet sich von einem lateinischen Wort ab, das “einnehmen” bedeutet. Es bezeichnet eine Verschreibung, die von einer zugelassenen medizinischen Fachkraft genehmigt werden muss.
S
- Sekundärverpackung: Dies ist die äußere Verpackung (Kartons und Schachteln), die die Primärverpackung abdeckt. Sie dient dem Schutz der Marke und des Arzneimittels während der Handhabung und des Versands.
- Strukturierte Produktkennzeichnung (SPL): Ein Dokumentauszeichnungsstandard für die Übermittlung von Produkt- und Betriebsinformationen an die FDA.
- Sterilisation: Durch die Sterilisation werden alle Formen von Mikroorganismen, einschließlich Sporen, von einer Oberfläche, einem Gerät oder einem pharmazeutischen Produkt entfernt.
T
- Therapeutischer Index: Der therapeutische Index ist das Verhältnis zwischen der toxischen und der wirksamen Dosis eines Arzneimittels. Er gibt die Sicherheitsspanne eines Arzneimittels bei der klinischen Anwendung an.
U
- Gleichmäßigkeit der Dosis: Die Einheitlichkeit der Dosis gewährleistet, dass jede Einheit eines Arzneimittels die gleiche Menge des Wirkstoffs enthält.
V
- Validierungsbericht: Ein Validierungsbericht ist ein Dokument, in dem bestätigt wird, dass ein pharmazeutischer Prozess oder eine pharmazeutische Ausrüstung konsistent Ergebnisse liefert, die den Qualitätsstandards entsprechen.
W
- Großhändler für Arzneimittel/3PL-Registrierung: Dies ist eine SPL-Vorlage, die von Unternehmen verlangt wird, die an der Lagerung und Verteilung von Arzneimitteln durch Dritte beteiligt sind.
- Nassgranulierung: Bei der Tablettenherstellung werden Pulver mit einem flüssigen Bindemittel gemischt, um ein Granulat zu bilden.
X
- Xenobiotika: Ein Xenobiotikum ist eine fremde chemische Verbindung, z. B. ein Medikament, ein Pestizid oder eine synthetische Chemikalie, die normalerweise nicht im Organismus vorhanden ist.
Y
- Berechnung der Ausbeute: Die Berechnung der pharmazeutischen Ausbeute ist das Verhältnis von Eingangsmaterialien zu Ausgangsprodukten und wird in Prozenten gemessen.
Z
- Null-Ordnung-Kinetik: Die Kinetik nullter Ordnung beschreibt die Eliminierung von Arzneimitteln mit einer konstanten Geschwindigkeit, die unabhängig von ihrer Plasmakonzentration ist.
Nehmen Sie teil an der Entwicklung der pharmazeutischen Industrie
Die Terminologie der Pharmaindustrie ist nicht der einzige Bereich, der sich weiterentwickelt; auch die Herstellung von Arzneimitteln entwickelt sich in einem noch nie dagewesenen Tempo. Jeden Tag werden neue Technologien eingeführt, von automatisierten Produktionslinien bis hin zu intelligenten Qualitätsüberwachungssystemen.
Im Zuge der Weiterentwicklung der Industrie reicht es nicht mehr aus, nur die Vorschriften einzuhalten. Unternehmen brauchen fortschrittliche, zuverlässige Fertigungssysteme, um an der Spitze zu bleiben, und das ist genau das, was Finetech in den letzten 30 Jahren geliefert hat.
Von hochmoderner Ausrüstung bis hin zu Maschinenschulung vor Ort, Wir helfen Pharmaherstellern dabei, ihre Produktion zu maximieren, die Einhaltung von Vorschriften zu gewährleisten und ihren Betrieb zukunftssicher zu machen.
Nehmen Sie jetzt Kontakt mit uns auf und erfahren Sie, wie Finetech Ihren Fertigungsprozess verändern kann.
Referenzen:
Ein Glossar für alle Begriffe Pharma.
Drugs@FDA Glossar der Begriffe.
Copyright-Hinweis:
Es ist nicht gestattet, Inhalte dieser Website zu vervielfältigen, zu verändern, zu veröffentlichen, darzustellen, zu übermitteln oder in irgendeiner Weise zu verwerten oder solche Inhalte zum Aufbau von Datenbanken jeglicher Art zu verwenden, es sei denn, es liegt eine ausdrückliche schriftliche Genehmigung der Finetech Group vor. Für eine Genehmigung zur Nutzung des Inhalts wenden Sie sich bitte an: info@pharmamachinecn.com
Haftungsausschluss:
Die in diesem Artikel enthaltenen Informationen dienen lediglich der allgemeinen Information. Das Unternehmen übernimmt keine Garantie für die Richtigkeit, Relevanz, Aktualität oder Vollständigkeit der Informationen, und das Unternehmen übernimmt keine Verantwortung für Fehler oder Auslassungen im Inhalt dieses Artikels.