Ligne de granulation pour formes posologiques solides
Notre ligne de granulation de comprimés solides est une technologie majeure pour les formes posologiques solides. Elle répond à des exigences techniques élevées pour les poudres et les granulés de médicaments avant leur mise en œuvre. former des comprimés et des capsules. C'est pourquoi Finetech vous propose une forme posologique solide complète solution pharmaceutique, applicable aux usines pharmaceutiques, de soins de santé et alimentaires.

Besoin d'un devis personnalisé
Pour plus d'informations sur ce produit, contactez notre équipe commerciale dès aujourd'hui !
Caractéristiques principales
FAQ
Application
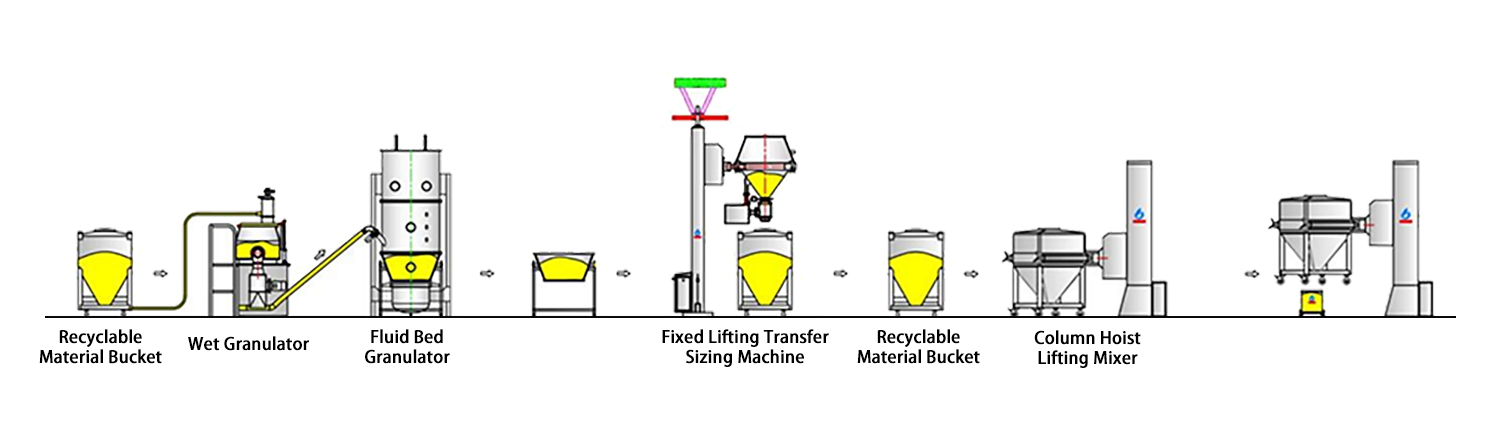
équipement de ligne de granulation
Commentaires Pas encore de commentaires
La ligne de granulation de Finetech est une technologie hautement fonctionnelle pour la production formes posologiques solides pharmaceutiques. Les exigences de qualité strictes concernant l'uniformité du contenu des granulés formés et leurs propriétés physicochimiques rendent crucial le choix du procédé adapté. La granulation humide garantit la transformation de mélanges hétérogènes de poudre fine en granulés uniformes. des particules de plus grande taille et une densité plus élevée.
Plage de capacité : 25L à 1 500L
Procédé de granulation : granulation humide et séchage fluidisé
Granulation humide : Utilise des liants liquides (par exemple, eau, éthanol).
Granulation à sec : Compactage (compactage au rouleau/slugging).
Granulation par fusion : Liants thermoactivables (par exemple, PEG).
Mouillé: Pour les poudres cohésives, améliore la fluidité.
Sec: Pour les API sensibles à l'humidité (évite la chaleur/le liquide).
Fondre: Pour les API thermostables avec des liants thermoplastiques.
Commencer avec 5–20% solution de liant (varie selon la formulation).
Ajustez la pression de la buse/le motif de pulvérisation pour une couverture uniforme.
Trop dur : Liant excessif/surgranulation.
Trop mou : Liant insuffisant/sous-séchage.
Ajuster la taille de l'écran de fraisage (plus petit = granulés plus lisses).
Ajouter des glissants (par exemple, silice colloïdale) dans le mélange final.
Après chaque lot (exigences GMP).
Nettoyage en profondeur hebdomadaire (démonter les pièces de contact).
BPF/OMS pour les produits pharmaceutiques.
ATEX (pour atmosphères explosives).
FDA 21 CFR Partie 11 (si vous utilisez des enregistrements numériques).
DQ/QI/QO/QP (Conception/Installation/Qualification opérationnelle/Performance).
TAPOTER (Process Analytical Technology) pour une surveillance en temps réel.













Avis des clients
Il n'y a pas encore de commentaires. Soyez le premier à commenter ce produit !