La terminologie pharmaceutique est un ensemble de termes techniques et de jargons complexes et spécifiques à l'industrie. Ces termes décrivent les normes, les processus et les réglementations qui assurent la cohérence du développement médical à l'échelle mondiale.

Connaître la bonne terminologie pharmaceutique donne de la crédibilité à votre voix. Elle vous aide à communiquer avec les médecins, les pharmaciens, les scientifiques, les distributeurs et les fournisseurs. Tout cela ouvre la voie à des décisions éclairées et à une collaboration productive dans l'ensemble du secteur.
Pour vous aider, nous vous présentons la terminologie la plus importante de l'industrie pharmaceutique que tout professionnel doit connaître.
UN
- Ingrédient pharmaceutique actif: An API est le cœur de tout médicament et délivre l'effet thérapeutique du médicament. Il s'associe à d'autres composants pour diagnostiquer, traiter, guérir ou prévenir une maladie.
- Ampoule : Petits récipients en verre scellés utilisés pour les médicaments injectables stériles. Ils protègent les liquides sensibles de l'air et de la contamination.
- Coût d'acquisition réel: Le CAA est le prix final payé par une pharmacie pour l'achat d'un médicament après les remises, les rabais, les rétrocessions et autres ajustements.
- ANDA (Abbreviated New Drug Application) : Une ANDA est soumise à la FDA pour obtenir l'approbation d'une version générique d'un médicament déjà approuvé en prouvant sa bioéquivalence.
B
- Emballage sous blister: Le emballage sous blister Les machines scellent chaque comprimé ou gélule dans sa propre cavité à l'aide de plastique et de papier d'aluminium.
- Biodisponibilité: La biodisponibilité mesure la quantité d'un médicament qui atteint la circulation sanguine. Elle dépend des propriétés physiques et chimiques du médicament, de la voie d'administration, de l'absorption, du métabolisme et de l'excrétion.
- Bioéquivalence: Elle compare la formulation et la biodisponibilité de deux médicaments afin de déterminer s'ils offrent les mêmes avantages thérapeutiques.
C
- Essai clinique : Les essais cliniques permettent de tester la sécurité et l'efficacité d'un nouveau médicament en vue de son approbation par la FDA.
- Médicaments contrefaits: Il s'agit de faux médicaments ou de médicaments produits illégalement, qui peuvent être nocifs pour la santé des consommateurs.
- Capsule : UN capsule est une forme de dosage qui contient l'IPA à l'intérieur d'une enveloppe de gélatine ou d'une enveloppe à base de plantes. L'enveloppe se dissout dans le tractus gastro-intestinal et le médicament est libéré dans la circulation sanguine.
- CCP (points de contrôle critiques) : Les CCP mettent en évidence les étapes clés du processus de fabrication où le contrôle est crucial pour prévenir la contamination et les problèmes de santé et de sécurité qui en découlent.
D
- Distributeur: Les distributeurs stockent, gèrent et livrent les médicaments et font le lien entre les fabricants et les vendeurs.
- DMF (Drug Master File) : Une DMF est une soumission confidentielle à la FDA. Elle comprend des informations sur les processus de fabrication, les matières premières, les installations, les matériaux d'emballage et d'autres données pertinentes.
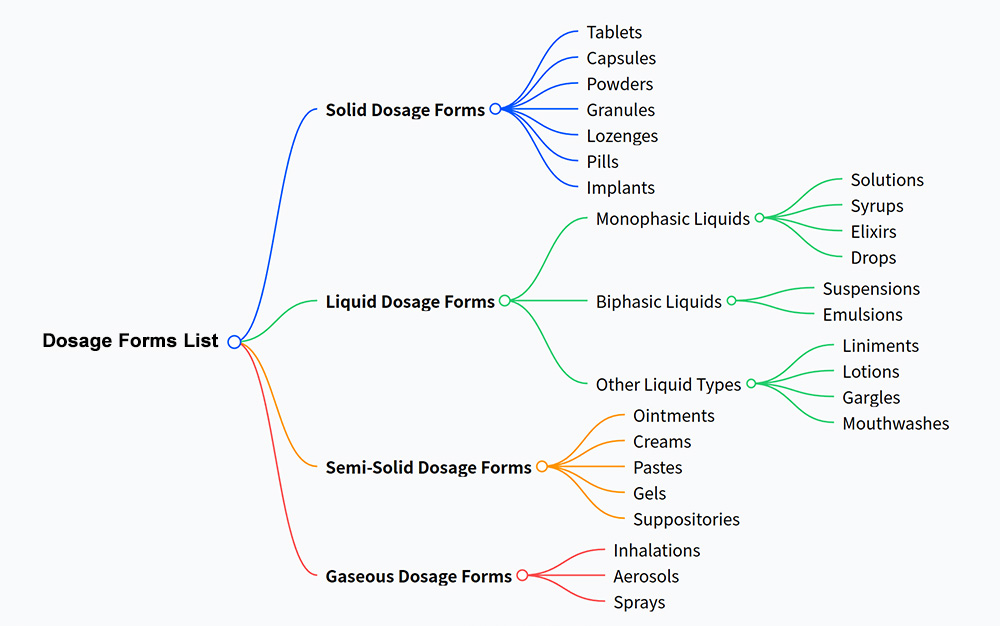
- Forme posologique: Il s'agit de la forme physique sous laquelle un médicament est produit et administré, comme les comprimés, les gélules, les pommades ou les sirops.
- Produit pharmaceutique: Le produit pharmaceutique est la forme de dosage finie contenant un ingrédient pharmaceutique actif (IPA) ainsi que des composants inactifs (excipients).
E
- Excipient: Les excipients sont des composants inactifs qui stabilisent et améliorent les propriétés de l'IPA.
- Date d'expiration: Date limite jusqu'à laquelle le médicament reste efficace et sûr dans les conditions de stockage recommandées.
- Endotoxine: Les endotoxines sont des substances toxiques libérées par le système immunitaire. membrane externe des bactéries Gram-négatives.
F
- FDA: La FDA est l'organisme de réglementation américain chargé de garantir la sécurité et l'efficacité des médicaments, des dispositifs médicaux, des produits biologiques et des produits alimentaires.
- Formulation: C'est le processus qui consiste à combiner des ingrédients actifs et inactifs pour créer un produit final stable et thérapeutiquement sûr.
- Produit fini: La forme finale d'un produit pharmaceutique qui a subi toutes les étapes de fabrication, de test de qualité et d'emballage.
G
- Médicament générique : Médicaments génériques contenir le même ingrédient pharmaceutique actif (IPA) et la même bioéquivalence que le médicament de marque.
- BPF (bonnes pratiques de fabrication) : Le BPF fournit un cadre pour la formulation, le traitement et l'emballage d'un médicament. Les règlements garantissent que tous les médicaments nouveaux et actuels répondent aux normes de sécurité afin de protéger la santé des patients.
- Bonnes pratiques cliniques (BPC) : Les BPC sont une norme internationale de qualité éthique et scientifique pour les essais cliniques impliquant des sujets humains.
H
- Homogénéité: La distribution uniforme de tous les composants dans une formulation est appelée homogénéité.
- Demi-vie: La demi-vie est le temps nécessaire pour que la concentration d'un médicament dans l'organisme diminue de moitié par rapport à son niveau initial.
I
- Identification des médicaments (IDMP) :Il se compose de cinq normes établies par l'ISO pour garantir une identification cohérente des médicaments dans le monde entier.
- Demande de nouveau médicament expérimental (IND): Il s'agit d'une demande soumise à la FDA en vue d'obtenir l'autorisation d'effectuer des essais cliniques sur l'homme d'un médicament expérimental.
- Intermédiaire: Les intermédiaires sont des composés chimiques produits lors de la fabrication d'un IPA. Ils subissent d'autres réactions chimiques pour devenir l'ingrédient pharmaceutique actif (IPA) fini.
J
- Fabrication juste à temps: Il s'agit d'une stratégie de production qui minimise les déchets et les coûts de stockage en ne fabriquant les produits pharmaceutiques que lorsqu'ils sont nécessaires.
K
- Kétamine: Il s'agit d'un anesthésique utilisé pour l'anesthésie dissociative, le traitement de la douleur et la dépression.
L
- Rapport sur la distribution des lots: Rapport soumis à la FDA pour indiquer la quantité de produits pharmaceutiques distribués dans le cadre de la demande de licence de produits biologiques (BLA).
- Lyophilisation: La lyophilisation est un procédé utilisé pour éliminer l'humidité des produits pharmaceutiques, principalement par congélation et sublimation, afin d'améliorer leur stabilité et leur durée de conservation.
M
- Dispositifs médicaux: Les dispositifs médicaux sont des instruments, des appareils, des implants et d'autres équipements connexes utilisés à des fins médicales.
- Procédure de reconnaissance mutuelle (PRM) : La procédure de reconnaissance mutuelle (PRM) est une procédure réglementaire européenne qui permet à un produit pharmaceutique autorisé dans un État membre de l'UE d'obtenir une approbation dans d'autres États.
N
- Nouvelle entité moléculaire : Un nouveau médicament qui contient un ingrédient actif qui n'a jamais été approuvé par la FDA auparavant.
O
- Médicaments en vente libre (OTC): Les médicaments qui peuvent être achetés en pharmacie sans ordonnance sont appelés médicaments en vente libre.
- Livre orange: Le Livre orangeest une publication de la FDA qui répertorie les médicaments approuvés et leur équivalence thérapeutique.
P
- Emballage primaire: L'emballage primaire (ampoules, flacons, blisters), également appelé emballage de vente, est le premier matériau en contact direct avec le médicament.
- Brevet: Un brevet accorde à une entreprise des droits exclusifs de fabrication et de vente d'un nouveau médicament, généralement pour une durée de 20 ans.
Q
- Contrôle de la qualité (CQ) : Il s'agit d'un système de test, d'inspection et de conformité réglementaire visant à détecter et à prévenir les défauts dans la production pharmaceutique.
- Assurance de la qualité (AQ)) : L'AQ est un processus systématique qui supervise chaque étape de la production pharmaceutique afin de s'assurer que les produits répondent aux normes de qualité.
R
- Rx : Il s'agit d'un symbole dérivé d'un mot latin qui signifie “prendre”. Il indique une prescription qui nécessite l'autorisation d'un professionnel de santé agréé.
S
- Emballage secondaire: Il s'agit de l'emballage extérieur (cartons et boîtes) qui recouvre l'emballage primaire. Il contribue à l'image de marque et à la protection des médicaments pendant la manipulation et l'expédition.
- Étiquetage structuré des produits (SPL) : Norme de balisage des documents pour la soumission d'informations sur les produits et les installations à la FDA.
- Stérilisation: La stérilisation permet d'éliminer toutes les formes de micro-organismes, y compris les spores, d'une surface, d'un équipement ou d'un produit pharmaceutique.
T
- Index thérapeutique : L'indice thérapeutique est le rapport entre la dose toxique et la dose efficace d'un médicament. Il indique la marge de sécurité d'un médicament lors de son utilisation clinique.
U
- Uniformité de la dose: L'uniformité de la dose garantit que chaque unité d'un médicament contient la même quantité de principe actif.
V
- Rapport de validation : Un rapport de validation est un document confirmant qu'un processus ou un équipement pharmaceutique produit régulièrement des résultats conformes aux normes de qualité.
W
- Enregistrement des distributeurs de médicaments en gros/3PL : Il s'agit d'une soumission SPL requise par les entreprises impliquées dans le stockage et la distribution de médicaments par des tiers.
- Granulation humide: Il s'agit d'un processus de fabrication de comprimés qui consiste à mélanger des poudres avec un liant liquide pour former des granulés.
X
- Xénobiotique: Un xénobiotique est un composé chimique étranger, tel qu'un médicament, un pesticide ou un produit chimique synthétique qui n'est pas habituellement présent dans l'organisme.
Y
- Calcul du rendement: Le calcul du rendement pharmaceutique est le rapport entre les matières entrantes et les produits sortants et est mesuré en pourcentage.
Z
- Cinétique de l'ordre zéro: La cinétique d'ordre zéro décrit l'élimination d'un médicament à une vitesse constante, indépendamment de sa concentration plasmatique.
Participez à l'évolution de l'industrie pharmaceutique
La terminologie de l'industrie pharmaceutique n'est pas la seule à se développer ; le secteur de la fabrication évolue à un rythme sans précédent. Chaque jour, de nouvelles technologies sont introduites, des lignes de production automatisées aux systèmes intelligents de contrôle de la qualité.
À mesure que l'industrie évolue, il ne suffit plus de rester conforme. Les entreprises ont besoin de systèmes de fabrication avancés et fiables pour garder une longueur d'avance, et c'est exactement ce qu'elles font. technologies fines depuis 30 ans.
De l'équipement de pointe à la formation à la machine sur site, En tant qu'experts, nous aidons les fabricants de produits pharmaceutiques à maximiser leur production, à maintenir leur conformité et à assurer la pérennité de leurs opérations.
Contactez-nous dès maintenant et découvrez comment Finetech peut transformer votre processus de fabrication.
Références :
Glossaire de tous les termes Pharma.
Glossaire des termes de Drugs@FDA.
Avis de droit d'auteur :
Vous ne pouvez pas reproduire, modifier, publier, afficher, transmettre ou exploiter de quelque manière que ce soit le contenu de ce site web, ni utiliser ce contenu pour constituer une base de données de quelque nature que ce soit, sans l'autorisation écrite expresse et préalable de Finetech Group. Pour obtenir l'autorisation d'utiliser le contenu, veuillez contacter : info@pharmamachinecn.com
Clause de non-responsabilité:
Les informations contenues dans cet article sont fournies à titre d'information générale uniquement. L'entreprise ne garantit pas l'exactitude, la pertinence, l'actualité ou l'exhaustivité des informations, et l'entreprise n'assume aucune responsabilité en cas d'erreur ou d'omission dans le contenu de cet article.